Cada año en todo el mundo, alrededor de 700 mil personas mueren a causa de infecciones causadas por varios tipos de bacterias resistentes a los antibióticos existentes en la actualidad.
A continuación se muestran algunos ejemplos: Una fractura abierta provocó que una mujer tuviera una infección en el fémur. Se utilizó terapia con antibióticos para el tratamiento, pero no tuvo éxito y el paciente murió de shock séptico. Más tarde se descubrió que Klebsiella, una bacteria de la flora humana normal, era patógena y resistente a los 26 antibióticos registrados en los Estados Unidos de América.
Cada año, alrededor de 23 mil personas en los Estados Unidos, 25 mil personas en Europa y alrededor de 700 mil personas en todo el mundo mueren por enfermedades infecciosas causadas por bacterias resistentes a los antibióticos. Según los expertos, en unas tres décadas, la tasa de muerte por tales bacterias alcanzará los 10 millones de personas al año. Sin embargo, la financiación para el desarrollo de nuevos antibióticos está disminuyendo.
Entonces, ¿por qué las bacterias se vuelven agresivas y resistentes a los medicamentos? ¿Y por qué, entonces, no es rentable el desarrollo de nuevos antibióticos?
norte
Como saben, los antibióticos se descubrieron por accidente. Alexander Fleming se destacó por su descuido, que no pinta en absoluto a un científico, y más aún a un bacteriólogo. En 1922, después de que el moco de su nariz penetrara en una colonia de bacterias, un científico descubrió accidentalmente una enzima llamada lisozima. Y 6 años después, en 1928, también introdujo accidentalmente esporas de moho en el cultivo de estafilococos y notó que todas las bacterias alrededor del hongo crecido habían muerto.
El científico llegó a la conclusión de que gracias al moho se sintetiza una sustancia bactericida al desplazar bacterias que compiten por un medio nutritivo. Fleming aisló penicilina del moho, que resultó ser más eficaz que los antisépticos externos que se usaban en cirugía en ese momento. La penicilina, a diferencia de los medicamentos antisépticos, se puede inyectar en el cuerpo humano y allí combate las infecciones en varios tejidos y órganos. Además, incluso después de que el fármaco se diluyó 800 veces, su actividad antibacteriana persistió.
Posteriormente, la alta actividad de pequeñas dosis del fármaco se explicó al determinar el mecanismo de acción de la penicilina. Cuando se utilizan antisépticos en altas concentraciones, se destruyen las paredes celulares de las bacterias. La penicilina, por otro lado, penetra en la célula, donde bloquea la formación de un biopolímero, que es necesario para el crecimiento de las paredes celulares bacterianas.
Sin embargo, muy pronto Fleming pudo establecer que si se administra una dosis demasiado pequeña de penicilina o se administra durante un período corto de tiempo, las colonias de bacterias que han logrado sobrevivir adquieren resistencia a aquellas dosis del fármaco que antes eran efectivas. E incluso más tarde, los científicos determinaron que los estafilococos tienen una capacidad innata para sintetizar una enzima que destruye la penicilina. Es, hasta cierto punto, un antídoto.
Video promocional:
Actualmente, los científicos han establecido de manera fehaciente que tales enfrentamientos son característicos no solo en condiciones naturales entre bacterias y hongos, sino también entre especies de bacterias del mismo género, ya que en este caso tienen el mismo sustrato y nicho por el que se debe luchar. Entonces, por ejemplo, en la actualidad, varios tipos de estafilococos luchan por la membrana mucosa de la boca humana, al mismo tiempo que producen antídotos y sustancias bactericidas.
Sin embargo, no hay ganadores ni perdedores en este enfrentamiento, ya que a lo largo de millones de años tal lucha evolutiva de muchos tipos de microorganismos de la microflora humana se convirtió en un equilibrio que se convirtió en una adquisición invaluable para el organismo en su conjunto. El número de cada especie está estrictamente limitado por la actividad bactericida de otros tipos de bacterias, el tamaño del nicho ocupado y la inmunidad del cuerpo. En particular, la población de Staphylococcus aureus, que causa infecciones purulentas, puede alcanzar hasta 10 mil bacterias por ml de medio sin dañar el cuerpo humano, y la bacteria Klebsiella puede estar presente en los intestinos o en la piel de una persona sana, y no dañar a una persona si el tamaño de la población No habrá más de 10 mil bacterias por gramo de heces.
Un ejemplo sencillo ayudará a responder la pregunta de por qué las bacterias adquieren una superresistencia a los antibióticos. En particular, uno puede imaginar que se está produciendo un conflicto en uno de los pequeños estados africanos y una de las partes recibió armas de destrucción masiva. Si hablamos de bacterias, los antibióticos se convertirán en tales armas de destrucción masiva, pero no de origen natural, sino sustancias sintéticas modernas que se utilizan en altas concentraciones.
Después del uso de tales antibióticos, debido a las especies de bacterias más sensibles al fármaco, habrá una reducción en la diversidad de especies. Los nichos que quedarán desocupados como resultado serán ocupados rápidamente por aquellos tipos de bacterias que tienen la capacidad de sintetizar antídotos. Por tanto, la ventaja evolutiva se dará a las colonias de las bacterias resistentes a los antibióticos y, como resultado, la diversidad genética dentro de una especie disminuirá. Por lo tanto, al usar antibióticos, una persona crea inconscientemente condiciones positivas para las cepas de bacterias más resistentes. Es por esta razón que el uso indiscriminado de antibióticos a menudo conduce al desarrollo de enfermedades crónicas provocadas por un aumento de la microflora patógena.
Una persona que sea portadora de este tipo de bacterias se convertirá en distribuidora, transmitiéndolas a sus familiares, amigos y conocidos, quienes eventualmente comenzarán a usar otros antibióticos. Así, la selección natural continuará y las bacterias que hayan sido resistentes a un tipo de antibiótico adquirirán gradualmente la denominada multirresistencia, es decir, resistencia a varios tipos de antibióticos. Son estos patógenos los que se llaman superbacterias.
norte
Además, muchos tipos de bacterias tienen la capacidad de intercambiar genes de resistencia mediante un plásmido (transferencia horizontal de elementos genéticos fuera del cromosoma). El gran peligro radica en el hecho de que las bacterias anaeróbicas, que se caracterizan por un metabolismo anóxico, adquieren resistencia a una gran cantidad de tipos de antibióticos. Si una persona se lesiona, estas bacterias pueden ingresar al torrente sanguíneo y causar una infección grave. Esto es exactamente lo que sucedió en el caso descrito anteriormente, cuando las bacterias penetraron en el tejido óseo. En un intento por salvar a la mujer, los médicos usaron casi una docena de antibióticos y se probaron una docena de medicamentos más en un cultivo aislado del foco de la infección, pero todos estos antibióticos fueron ineficaces.
Un peligro aún mayor es que todo tipo de bacterias patógenas pueden adquirir resistencia a los antibióticos, en particular las que causan ántrax, salmonelosis y disentería. Aunque todas estas infecciones son prácticamente infrecuentes, sus patógenos pueden adquirir fácilmente resistencia a los antibióticos de las bacterias de la microflora normal debido a la transferencia horizontal de genes en los plásmidos. Además, los animales de granja suelen ser portadores de infecciones peligrosas. Cabe señalar que en este caso, las bacterias resistentes están mucho más extendidas en ellos que en los humanos. Según los expertos, esto se debe a que en la agricultura se añaden antibióticos a la alimentación para prevenir diversos tipos de infecciones. Estas dosis no matan las bacterias,pero solo no dejes que se multipliquen. Pero después de todo, Fleming dijo que el uso de dosis bajas de antibióticos conduce a una disminución de la sensibilidad a los medicamentos.
Un experimento muy interesante fue realizado por un grupo de investigadores de Harvard, en el que se mostró cómo crece el número de cepas resistentes de bacterias en el caso de un aumento gradual de la concentración de antibióticos de un mínimo a mil veces.
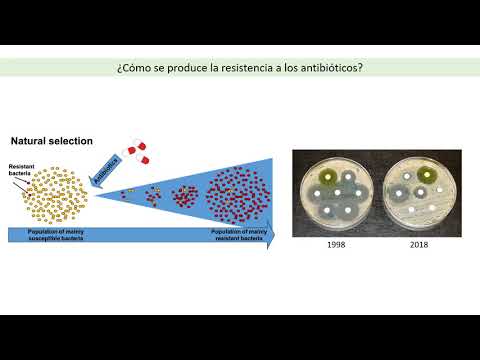
Por lo tanto, los antibióticos solo deben tomarse según lo prescrito por los médicos y solo en las dosis recomendadas. Al mismo tiempo, debe recordarse que si la bacteria que provocó la enfermedad ya es resistente al antibiótico, incluso tomar el medicamento en altas concentraciones durante mucho tiempo puede ser ineficaz. En este caso, es necesario determinar en condiciones de laboratorio la sensibilidad de la bacteria al fármaco. Para ello, junto con la inoculación de bacterias, se colocan discos de papel sobre el medio nutritivo, que se impregnan con diversos tipos de antibióticos. Cuando aparecen anillos transparentes alrededor de los discos, podemos hablar de la ausencia de crecimiento de cultivos bacterianos. En otras palabras, es sensible a este antibiótico. En ausencia de un anillo transparente, podemos hablar de la presencia de resistencia.
Gracias a los resultados de dicho estudio, los médicos ya podrán prescribir uno de los antibióticos de espectro estrecho, suprimiendo el patógeno sin dañar toda la microflora. Sin embargo, este tipo de investigación es bastante costosa y requiere varios días. Por esta razón, para no perder el tiempo, los médicos, por regla general, recetan antibióticos sin esperar los resultados de la prueba. En la mayoría de los casos, este análisis no se realiza en absoluto y el antibiótico se prescribe sin determinar el tipo de patógeno. Por tanto, se utiliza un antibiótico de amplio espectro. Esto puede tener un efecto positivo en algunos casos, pero a escala humana, esta práctica empeora aún más el problema de la resistencia bacteriana a los antibióticos.
Si hablamos del desarrollo y prueba de nuevos tipos de antibióticos, cabe señalar que este proceso es muy laborioso y caro. Su implementación requiere alrededor de mil millones de dólares de inversión y más de diez años. Además, los antibióticos se utilizan en la mayoría de los casos en cursos cortos, a veces solo unas pocas veces en la vida. Si hablamos de fármacos antipiréticos, analgésicos u hormonales, se utilizan con mucha más frecuencia y de forma más amplia. Esto, a su vez, los hace más atractivos para las inversiones. Debido a esto, cada vez se introducen menos en la práctica nuevos antibióticos.
La renuencia de los inversores a invertir en el desarrollo de nuevos fármacos también se debe al hecho de que la resistencia de las últimas generaciones de bacterias está aumentando cada vez más. En la terapia moderna, los médicos se abstienen del uso generalizado de nuevos antibióticos, usándolos solo en casos extremos en forma de reserva. Esto reduce la demanda de estas drogas y las priva de ganancias. Por tanto, resulta que la resistencia bacteriana provocada por los antibióticos inhibe el desarrollo de nuevos fármacos.
Sin lugar a dudas, el descubrimiento y uso activo de antibióticos en terapia se ha convertido en un verdadero avance en la medicina. Desde sus inicios, los antibióticos han salvado millones de vidas humanas. Pero ahora es necesario buscar nuevas soluciones que ayuden a reducir la dependencia de la medicina del uso de antibióticos.